GLP-1
GLP-1: il ponte tra glucosio, sazietà e peso corporeo
Nell’attuale panorama della salute metabolica, il GLP-1 occupa una posizione centrale. La sua crescente rilevanza nella comunità scientifica è stata evidenziata dallo sviluppo di farmaci che ne targettano il recettore. Tuttavia, al di là dell’applicazione terapeutica, emerge una domanda più profonda: qual è il ruolo del GLP-1 come regolatore del metabolismo?
Lontano dall’essere semplicemente un “ormone della perdita di peso”, il glucagon-like peptide-1 (GLP-1) è un integratore metabolico che collega la regolazione del glucosio, il controllo dell’appetito e l’equilibrio energetico (1,2). Comprendere questo asse consente di adottare una visione più sistemica del metabolismo.
Un ormone con una funzione coordinata
Il GLP-1 è un ormone incretinico prodotto dalle cellule enteroendocrine L, localizzate principalmente nell’ileo e nel colon. Dopo la secrezione, circola in due principali forme attive, GLP-1 (7–36) e GLP-1 (7–37), con un’emivita breve a causa della rapida degradazione da parte dell’enzima DPP-IV (1).
La sua azione biologica dipende dal legame con il recettore del GLP-1 (GLP-1R), espresso in diversi tessuti. L’attivazione di questo recettore innesca una segnalazione intracellulare dipendente dall’AMPc che (1,3):
Stimola la secrezione di insulina in modo glucosio-dipendente
Inibisce il rilascio di glucagone
Preserva la massa funzionale delle cellule β pancreatiche
Migliora l’omeostasi glicemica postprandiale
Questo meccanismo colloca il GLP-1 come modulatore centrale del controllo metabolico.
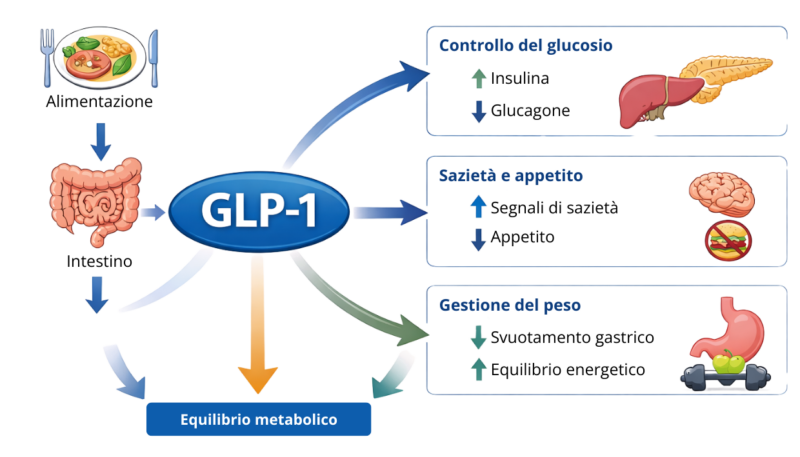
Schema concettuale basato su (Wang et al., 2021; Domínguez-Avila et al., 2017; Derosa et al., 2025).
Punto di partenza:
Regolazione del glucosio
Tra l’ampia attenzione mediatica verso analoghi del GLP-1 come semaglutide (Ozempic) e liraglutide (Saxenda), il dibattito pubblico si è concentrato principalmente sugli effetti sulla riduzione del peso corporeo. Tuttavia, questo focus ha in parte oscurato il ruolo fisiologico principale del GLP-1: la regolazione della glicemia postprandiale, cioè il controllo dell’aumento dei livelli di glucosio nel sangue dopo l’assunzione di cibo.
Una risposta glicemica postprandiale più stabile riduce sia la variabilità metabolica sia l’iperinsulinemia compensatoria, due fattori strettamente correlati allo sviluppo progressivo dell’insulino-resistenza e del diabete di tipo 2. In questo contesto, la questione critica non è solo l’entità dell’aumento di glucosio, ma l’efficienza con cui l’organismo lo regola e si adatta a tale incremento (2,4,5).
Il diabete di tipo 2 non compare bruscamente; si sviluppa gradualmente man mano che i tessuti periferici diventano meno sensibili all’insulina e le cellule β pancreatiche subiscono un progressivo declino funzionale. Quando questi processi convergono, il mantenimento dell’omeostasi glicemica viene compromesso.
In questo quadro, il sistema delle incretine, in particolare l’asse GLP-1/GLP-1R, assume un’importanza fisiologica significativa (1,3,6). Il GLP-1 potenzia la secrezione di insulina in modo glucosio-dipendente, amplificando la sua azione quando i livelli di glucosio aumentano dopo un pasto, mentre contemporaneamente sopprime il rilascio di glucagone. Questa risposta coordinata consente un adeguamento metabolico più fisiologico, contribuendo alla preservazione della funzione delle cellule β e al miglioramento della regolazione metabolica complessiva (1,6).
Di conseguenza, le strategie mirate a ottimizzare il controllo della glicemia postprandiale vanno oltre la semplice riduzione del peso. Esse puntano a migliorare la qualità e l’efficienza della risposta metabolica a ciascun pasto, un approccio con implicazioni più ampie per la prevenzione e la gestione a lungo termine dei disturbi metabolici (2,7,8).
GLP-1 e sazietà:
Il collegamento intestino-cervello
Oltre al suo ruolo nel controllo glicemico, il GLP-1 partecipa direttamente alla regolazione dell’appetito. Questo ormone rallenta lo svuotamento gastrico, prolungando la sensazione di sazietà dopo i pasti, e agisce sui neuroni ipotalamici che esprimono GLP-1R, modulando i segnali di sazietà e riducendo l’assunzione di cibo (1).
Questo effetto fa parte di un sistema di feedback che regola l’equilibrio energetico in base allo stato nutrizionale. Durante il digiuno, i livelli di grelina aumentano e stimolano l’appetito; dopo l’assunzione di cibo, la secrezione di GLP-1 cresce e contribuisce a ridurre questo segnale orexigenico. L’interazione reciproca tra questi ormoni riflette una regolazione coordinata dell’equilibrio energetico, dimostrando che il GLP-1 risponde non solo al glucosio, ma allo stato metabolico complessivo dell’organismo (1).
Microbiota and GLP-1
La fermentazione delle fibre alimentari da parte del microbiota intestinale genera acidi grassi a catena corta (SCFA), che possono modulare la secrezione di GLP-1 (6). Questa relazione rafforza il ruolo dell’intestino come organo endocrino chiave nella regolazione metabolica e pone l’interazione dieta–microbiota–incretina come un asse rilevante nella prevenzione cardiometabolica (8,9).
Regolazione della secrezione di GLP-1: un sistema multifattoriale
La secrezione di GLP-1 risponde a un sistema integrato di segnali neuronali e nutrizionali.
Dopo l’assunzione di cibo, si verifica una fase iniziale mediata dall’attivazione del nervo vago e da meccanismi neuroendocrini, seguita da una fase tardiva dipendente dal contatto diretto dei nutrienti con l’intestino (1). In quest’ultima fase, glucosio, acidi grassi, SCFA derivati dal microbiota e peptidi o amminoacidi stimolano le cellule L intestinali tramite recettori e trasportatori specifici (1,7).
Questo modello conferma che il GLP-1 funziona come sensore metabolico dell’assunzione di nutrienti.
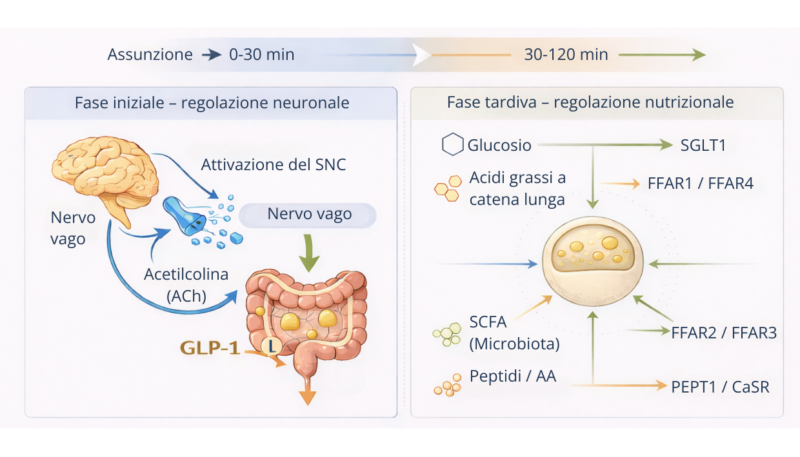
Adattato da (Wang et al., 2021; Domínguez-Avila et al., 2017; Iatcu et al., 2024).
Sebbene il suo ruolo principale sia il controllo glicemico, il GLP-1 esercita effetti anche in altri tessuti, con possibili implicazioni per la funzione epatica, la regolazione cardiovascolare e il metabolismo osseo (1). Nel complesso, l’asse GLP-1/GLP-1R può essere considerato un nodo integrativo che connette intestino, pancreas e sistema nervoso centrale nella regolazione dell’equilibrio metabolico.
Stai cercando gli ingredienti giusti?
Iscriviti alla nostra newsletter…
…oppure scopri i nostri ingredienti nel seguente portfolio di prodotti!
Riferimenti
- Wang Y, Alkhalidy H, Liu D. The emerging role of polyphenols in the management of type 2 diabetes. Molecules. 2021;26(3):703.
- Derosa G, et al. Nutraceuticals and supplements in the management of prediabetes and diabetes: Mechanistic and clinical evidence. Nutrients. 2025;17(1):14.
- Domínguez Avila JA, et al. The antidiabetic mechanisms of polyphenols related to increased GLP-1 and insulin signaling. Molecules. 2017;22(6):903.
- Lown M, Fuller R, Lightowler H, Fraser A, Gallagher A. Mulberry-extract improves glucose tolerance and decreases insulin concentrations in normoglycaemic adults: A randomized double-blind placebo-controlled study. PLoS ONE. 2017;12(2):e0172239.
- Thondre PS, Lightowler H, Ahlstrom L. Mulberry leaf extract improves glycaemic response to sucrose in healthy subjects: A randomized, double-blind, placebo-controlled study. Nutrition & Metabolism. 2021;18:42.
- Abiola JO, et al. Potential role of phytochemicals as GLP-1 receptor agonists in diabetes. Pharmaceuticals. 2024;17(6):736.
- Iatcu OC, et al. Harnessing prebiotics to improve type 2 diabetes outcomes: Mechanisms and clinical relevance. Nutrients. 2024;16(20):3447.
- Venkatakrishnan K, et al. Functional foods and nutraceuticals in obesity and metabolic disorders. Food & Function. 2019;10:1240–1263.
- Cevallos-Fernández E, et al. Fermented plant-based foods and postbiotics for glycemic control: Mechanistic insights and clinical implications. Frontiers in Nutrition. 2026.